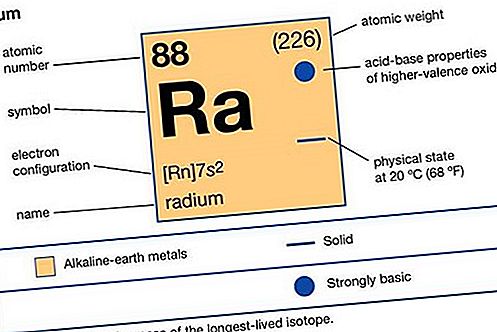
Ušlechtilý plyn, kterýkoli ze sedmi chemických prvků tvořících skupinu 18 (VIIIa) periodické tabulky. Prvky jsou helium (He), neon (Ne), argon (Ar), krypton (Kr), xenon (Xe), radon (Rn) a oganesson (Og). Ušlechtilé plyny jsou bezbarvé, bez zápachu, bez chuti a nehořlavé plyny. Tradičně byly v periodické tabulce označeny jako Skupina 0, protože po celá desetiletí po jejich objevení se věřilo, že se nemohou vázat na jiné atomy; to znamená, že jejich atomy se nemohly kombinovat s atomy jiných prvků za vzniku chemických sloučenin. Jejich elektronické struktury a zjištění, že některé z nich skutečně tvoří sloučeniny, vedly k vhodnějšímu označení, skupina 18.
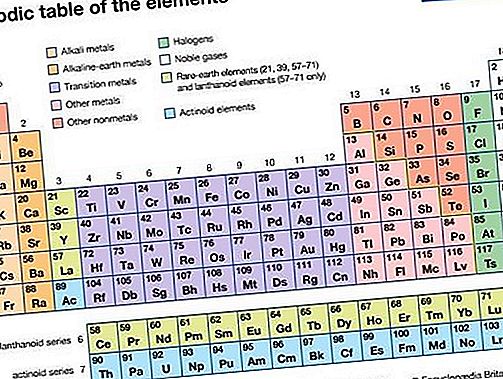
Když byli členové skupiny objeveni a identifikováni, považovali se za mimořádně vzácné a také chemicky inertní, a proto se jim říkalo vzácné nebo inertní plyny. Nyní je však známo, že několik z těchto prvků je na Zemi a ve zbytku vesmíru poměrně hojné, takže označení vzácné je zavádějící. Podobně použití pojmu inertní má tu nevýhodu, že představuje chemickou pasivitu, což naznačuje, že sloučeniny skupiny 18 nelze tvořit. V chemii a alchymii slovo šlechtice již dlouho znamenalo neochotu kovů, jako je zlato a platina, podstoupit chemickou reakci; to platí ve stejném smyslu pro skupinu plynů zde zahrnutých.
Množství vzácných plynů klesá se zvyšováním jejich atomových čísel. Hélium je nejhojnějším prvkem ve vesmíru kromě vodíku. Všechny vzácné plyny jsou přítomny v zemské atmosféře a kromě helia a radonu je jejich hlavním komerčním zdrojem vzduch, ze kterého se získávají zkapalněním a frakční destilací. Většina helia se vyrábí komerčně z určitých studní na zemní plyn. Radon je obvykle izolován jako produkt radioaktivního rozkladu sloučenin radia. Jádra atomů radia se spontánně rozkládají emitováním energie a částic, jader helia (alfa částice) a atomů radonu. Některé vlastnosti vzácných plynů jsou uvedeny v tabulce.
Některé vlastnosti ušlechtilých plynů
| hélium | neon | argon | krypton | xenon | radon | ununoctium | |
|---|---|---|---|---|---|---|---|
| * Při 25,05 atmosfér. | |||||||
| ** hcp = hexagonální těsně zabalený, fcc = krychlový centrovaný na tvář (krychlový těsně zabalený). | |||||||
| *** Nejstabilnější izotop. | |||||||
| protonové číslo | 2 | 10 | 18 | 36 | 54 | 86 | 118 |
| atomová hmotnost | 4,003 | 20.18 | 39,948 | 83,8 | 131,293 | 222 | 294 *** |
| teplota tání (° C) | −272,2 * | −248,59 | −189,3 | -157,36 | −111.7 | −71 | - |
| bod varu (° C) | −268,93 | −246,08 | −185,8 | -153,22 | -108 | -61,7 | - |
| hustota při 0 ° C, 1 atmosféra (gramy na litr) | 0,177847 | 0,899 | 1,784 | 3,75 | 5,881 | 9,73 | - |
| rozpustnost ve vodě při 20 ° C (kubický centimetr plynu na 1 000 gramů vody) | 8,61 | 10.5 | 33.6 | 59.4 | 108.1 | 230 | - |
| izotopová hojnost (pozemní, procento) | 3 (0,000137), 4 (99,999863) | 20 (90,48), 21 (0,27), 22 (9,25) | 36 (0,3336), 40 (99,6003) | 78 (0,35), 80 (2,28), 82 (11,58), 83 (11,49), 84 (57), 86 (17,3) | 124 (0,09), 126 (0,09), 128 (1,92), 129 (26,44), 130 (4,08), 131 (21,18), 132 (26,89), 134 (10,44), 136 (8,87) | - | - |
| radioaktivní izotopy (hmotnostní čísla) | 5–10 | 16–19, 23–34 | 30–35, 37, 39, 41–53 | 69–77, 79, 81, 85, 87–100 | 110–125, 127, 133, 135–147 | 195–228 | 294 |
| barva světla emitovaného plynnou výbojkou | žlutá | Červené | červená nebo modrá | žluto zelená | modrá až zelená | - | - |
| teplo fúze (kilojouly na mol) | 0,02 | 0,34 | 1.18 | 1,64 | 2.3 | 3 | - |
| odpařovací teplo (kalorie na mol) | 0,083 | 1,75 | 6.5 | 9.02 | 12,64 | 17 | - |
| měrné teplo (jouly na gram Kelvina) | 5.1931 | 1,03 | 0,52033 | 0,24805 | 0,155832 | 0,09365 | - |
| kritická teplota (K) | 5.19 | 44.4 | 150,87 | 209,41 | 289,77 | 377 | - |
| kritický tlak (atmosféry) | 2.24 | 27.2 | 48,34 | 54.3 | 57,65 | 62 | - |
| kritická hustota (gramy na krychlový centimetr) | 0,0696 | 0,4819 | 0,5356 | 0,9092 | 1,103 | - | - |
| tepelná vodivost (watty na metr Kelvin) | 0,1513 | 0,0491 | 0,0177 | 0,0094 | 0,0057 | 0,0036 | - |
| magnetická citlivost (cgs jednotky na mol) | −0,0000019 | -0,0000072 | -0,0000194 | -0,000028 | -0,000043 | - | - |
| Krystalická struktura** | hcp | fcc | fcc | fcc | fcc | fcc | - |
| poloměr: atomový (angstromy) | 0,31 | 0,38 | 0,71 | 0,88 | 1,08 | 1.2 | - |
| poloměr: odhad kovalentního (křišťálového) (angstromy) | 0,32 | 0,69 | 0,97 | 1.1 | 1.3 | 1,45 | - |
| statická polarizovatelnost (kubické angstromy) | 0,204 | 0,392 | 1,63 | 2,465 | 4,01 | - | - |
| ionizační potenciál (první, elektronové volty) | 24,587 | 21,565 | 15,759 | 13,999 | 12,129 | 10,747 | - |
| elektronegativita (Pauling) | 4.5 | 4.0 | 2.9 | 2.6 | 2.25 | 2,0 | - |