Rádium (Ra), radioaktivní chemický prvek, nejtěžší z kovů alkalických zemin skupiny 2 (IIa) periodické tabulky. Radium je stříbřitě bílý kov, který se v přírodě nevyskytuje volně.
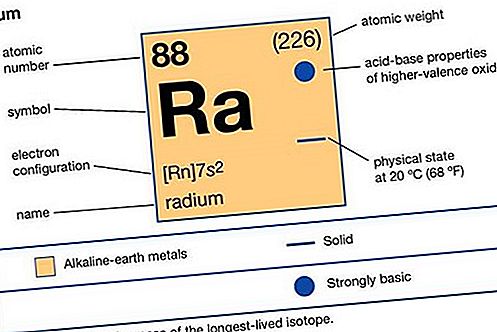

kov alkalických zemin
baryum (Ba) a radium (Ra).
Vlastnosti prvku
| protonové číslo | 88 |
|---|---|
| nejstabilnější izotop | 226 |
| bod tání | přibližně 700 ° C (1300 ° F) |
| bod varu | není dobře zavedeno (přibližně 1100–1 700 ° C [2 000–3 100 ° F]) |
| specifická gravitace | asi 5 |
| oxidační stav | +2 |
| elektronová konfigurace | [Rn] 7s 2 |
Výskyt, vlastnosti a použití
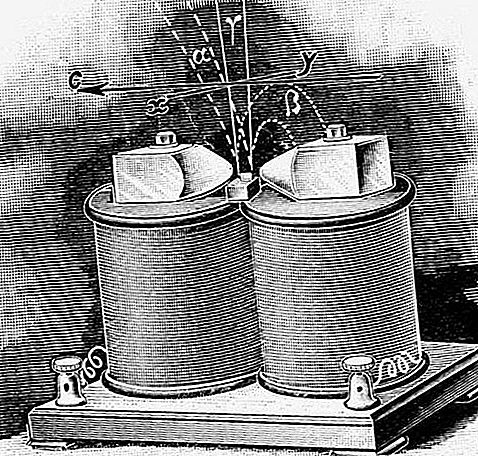
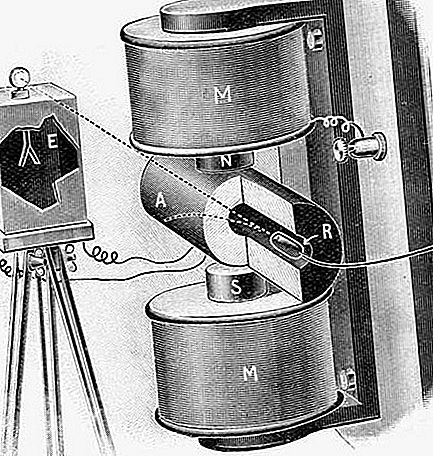
Rádium objevil (1898) Pierre Curie, Marie Curie a asistent G. Bémont poté, co Marie Curie zjistila, že radioaktivita pitchblende byla čtyřikrát až pětkrát větší než radioaktivita uranu, který obsahoval, a nebyla plně vysvětlena na na základě radioaktivního polonia, které právě objevila ve zbytcích smoly. Nová, silně radioaktivní látka mohla být koncentrována bariem, ale protože její chlorid byl o něco více nerozpustný, mohla být vysrážena frakční krystalizací. Po separaci následovalo zvýšení intenzity nových linií v ultrafialovém spektru a stálé zvýšení zdánlivé atomové hmotnosti materiálu, dokud nebyla získána hodnota 225,2, pozoruhodně blízko aktuálně akceptované hodnoty 226,03. V roce 1902 bylo připraveno 0,1 gramu čistého chloridu radiačního rafinováním několika tun zbytků smoly a do roku 1910 Marie Curie a André-Louis Debierne izolovali samotný kov.
Je známo třicet čtyři izotopů radia, všechny radioaktivní; jejich poločasy, s výjimkou radia 226 (1600 let) a radia 228 (5,75 let), jsou kratší než několik týdnů. Radium 226 s dlouhou životností se nachází v přírodě v důsledku jeho neustálé tvorby z rozkladu uranu-238. Radium se tak vyskytuje ve všech uranových rudách, ale je rozšířenější, protože tvoří sloučeniny rozpustné ve vodě; Zemský povrch obsahuje odhadem 1,8 x 10 13 g (2 x 10 7 tun) radia.
Protože všechny izotopy radia jsou radioaktivní a krátkodobé v geologickém časovém měřítku, jakékoli pravěké radium by dávno zmizelo. Proto se radium vyskytuje přirozeně pouze jako dezintegrační produkt ve třech přírodních radioaktivních rozpadových sériích (řada thoria, uranu a aktinia). Radium-226 je členem série rozkladu uranu. Jeho rodičem je thorium-230 a jeho dcera radon-222. Dalšími produkty rozkladu, dříve nazývanými radium A, B, C, C ', C ″, D atd., Jsou izotopy polonia, olova, bizmutu a thalia.








![Velký žárový film Lang [1953] Velký žárový film Lang [1953]](https://images.thetopknowledge.com/img/entertainment-pop-culture/0/big-heat-film-lang-1953.jpg)


