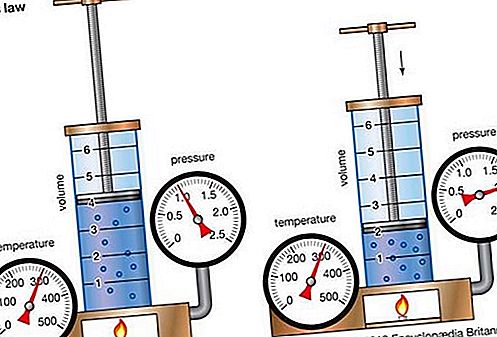
Boyleův zákon, také nazývaný Mariotteův zákon, vztah týkající se stlačování a expanze plynu při konstantní teplotě. Tento empirický vztah, formulovaný fyzikem Robert Boyle v roce 1662, uvádí, že tlak (p) daného množství plynu se mění nepřímo s jeho objemem (v) při konstantní teplotě; tj. ve formě rovnice, pv = k, konstanta. Vztah také objevil francouzský fyzik Edme Mariotte (1676).
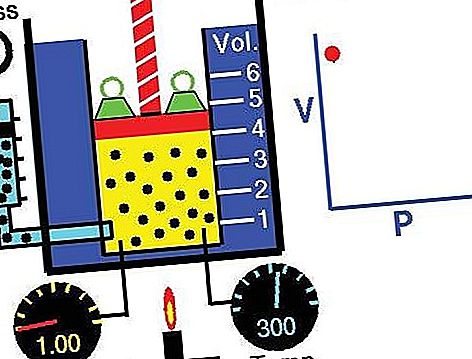
Zákon lze odvodit z kinetické teorie plynů za předpokladu dokonalého (ideálního) plynu (viz dokonalý plyn). Skutečné plyny dodržují Boyleův zákon při dostatečně nízkých tlacích, ačkoli produkt pv obecně klesá mírně při vyšších tlacích, kde se plyn začíná odchýlit od ideálního chování.