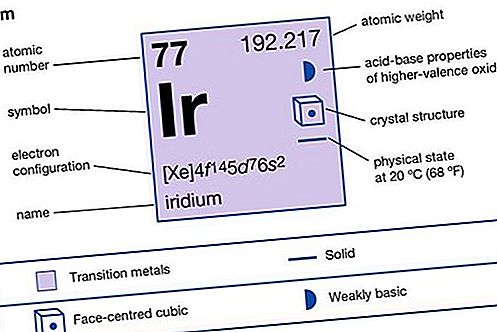
Iridium (Ir), chemický prvek, jeden z platinových kovů skupin 8–10 (VIIIb), období 5 a 6 periodické tabulky. Je velmi hustý a vzácný a používá se ve slitinách platiny. Iridium je drahý stříbrný bílý kov, který je tvrdý a křehký, ale stává se tažným a lze jej zpracovávat na bílém žáru, od 1 200 ° do 1 500 ° C (2 200 ° až 2 700 ° F). Je to jedna z nejhustších pozemních látek. V masivním stavu je kov prakticky nerozpustný v kyselinách a není ani napaden aqua regia. Může být rozpuštěn v koncentrované kyselině chlorovodíkové v přítomnosti chloristanu sodného při 125 ° až 150 ° C (257 ° až 302 ° F).
Vzhledem k obtížím při přípravě a výrobě má čistý kov jen několik použití. Iridium se používá hlavně ve formě platinových slitin. Slitiny platiny a iridia (5 až 10 procent iridia) jsou snadno zpracovatelné kovy, které jsou mnohem tvrdší a tužší a odolnější vůči chemickému napadení než měkká čistá platina. Takové slitiny se používají pro šperky, hroty per, chirurgické špendlíky a čepy a elektrické kontakty a body jisker. Mezinárodní prototypový standardní kilogram hmotnosti je vyroben ze slitiny obsahující 90 procent platiny a 10 procent iridia.
Čisté iridium se v přírodě pravděpodobně nevyskytuje; jeho hojnost v zemské kůře je velmi nízká, asi 0,001 dílu na milion. Ačkoli vzácný, iridium se vyskytuje v přírodních slitinách s jinými ušlechtilými kovy: v iridosmin až 77 procent iridium, v platiniridium až 77 procent, v aurosmiridium 52 procent a v nativní platině až 7,5 procent. Iridium se obecně vyrábí komerčně spolu s dalšími platinovými kovy jako vedlejší produkt při výrobě niklu nebo mědi.
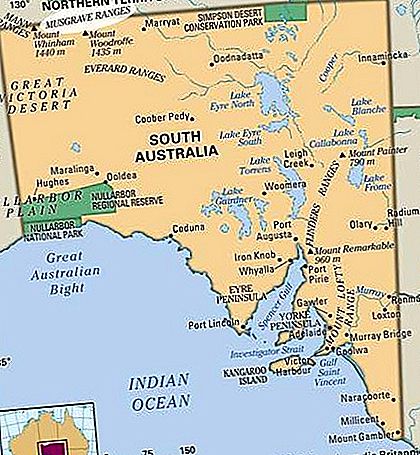
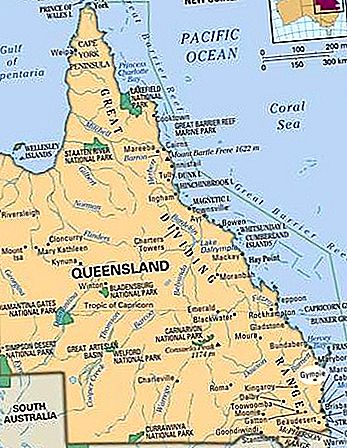
Rudy obsahující iridium se nacházejí v Jižní Africe a na Aljašce, v USA a také v Myanmaru (Barma), Brazílii, Rusku a Austrálii. Na konci 20. století byla Jižní Afrika největším producentem iridia na světě.
Tento prvek byl objeven v roce 1803 v kyselině nerozpustných zbytcích platinových rud anglickým chemikem Smithsonem Tennantem; francouzští chemici H.-V. Collet-Descotils, A.-F. Fourcroy a N.-L. Vauquelin to identifikoval přibližně ve stejnou dobu. Název iridium, odvozený z řeckého slova iris („duha“), označuje různé barvy jeho sloučenin. Přírodní iridium se skládá ze směsi dvou stabilních izotopů, iridia-191 (37,3 procenta) a iridia-193 (62,7 procenta). Chemie iridia se soustřeďuje na oxidační stavy +1, +3 a +4, ačkoli sloučeniny všech stavů od 0 do +6 jsou známé, snad s výjimkou +2. Komplexy v oxidačním stavu +1 obsahují hlavně ligandy jako oxid uhelnatý, olefiny a fosfiny. Anionty hexachloroiridát, [IrCl 6] 2 a hexabromoiridát, [IrBr 6] 2 -, jsou jediné významné chemické látky, které obsahují iridium v oxidačním stavu +4. Iridium je o něco reaktivnější než ruthenium a osmium.
Vlastnosti prvku
| protonové číslo | 77 |
|---|---|
| atomová hmotnost | 192,2 |
| bod tání | 2 410 ° C (4 370 ° F) |
| bod varu | 4 527 ° C (8 181 ° F) |
| specifická gravitace | 22,4 (20 ° C) |
| oxidační stavy | +1, +3, +4 |
| elektronová konfigurace. | [Xe] 4f 14 5d 9 |










![Quebec akt Velká Británie [1774] Quebec akt Velká Británie [1774]](https://images.thetopknowledge.com/img/politics-law-government/5/quebec-act-great-britain-1774.jpg)
