Anhydrid, jakákoli chemická sloučenina získaná, buď v praxi, nebo v zásadě, odstraněním vody z jiné sloučeniny. Příklady anorganických anhydridů jsou oxid sírový, SO 3, která je odvozena od kyseliny sírové a oxidu vápenatého, CaO, získané z hydroxidu vápenatého. Oxid sírový a další oxidy vytvářené odstraňováním vody z kyseliny se často nazývají anhydridy kyselin, zatímco oxidy vápníku, které jsou produkovány bází při ztrátě vody, se označují jako bazické anhydridy.
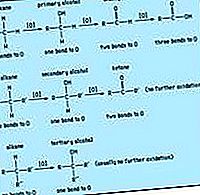
karboxylová kyselina: Anhydridy
Funkční skupina anhydridu karboxylové kyseliny jsou dvě acylové skupiny navázané na atom kyslíku. Anhydrid může být symetrický (dva stejné
Nejdůležitější z organických anhydridů je anhydrid kyseliny octové, (CH 3 CO) 2 O. Je připraven průmyslově jedním ze dvou způsobů: atmosférickou oxidací acetaldehydu v přítomnosti kovového acetátu; a z kyseliny octové reakcí s acetylenem nebo ketenem. Jiné organické anhydridy mohou být připraveny z karboxylových kyselin reakcí s acetanhydridem, ketenem, methoxyacetylenem nebo isopropenylacetátem. Anhydridy se také vyrábějí, když acylhalogenidy reagují s acetanhydridem nebo s karboxylovou kyselinou a pyridinem.
Organické anhydridy se používají k zavedení acylové skupiny (RCO) do organické syntézy. Reagují s vodou za vzniku karboxylových kyselin, s alkoholy nebo fenoly za vzniku esterů, s amoniakem a aminy za vzniku amidů. Acetanhydrid se používá při výrobě acetátu celulózy, který se široce používá jako základ pro magnetickou pásku a při výrobě textilních vláken. Rovněž se zahřívá kyselinou salicylovou za vzniku léčivé chemické kyseliny acetylsalicylové (aspirin).