Scandium (Sc), chemický prvek, kov vzácných zemin skupiny 3 periodické tabulky.
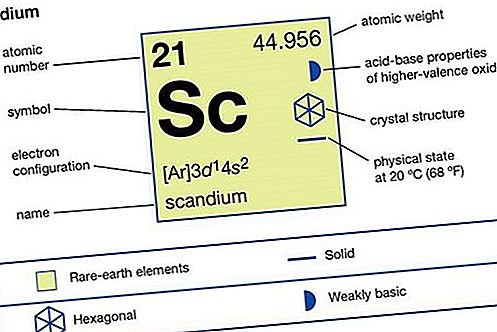
Scandium je stříbřitě bílý, středně měkký kov. To je poměrně stabilní na vzduchu, ale pomalu změní barvu z stříbřitý bílý až žlutavý vzhled, protože tvoření Sc 2 O 3, oxidu na povrchu. Kov se pomalu rozpustí ve zředěných kyselinách - s výjimkou kyseliny fluorovodíkové (HF), ve které ochranná trifluoridová vrstva brání další reakci. Skandium je paramagnetické od 0 K (- 273 ° C nebo -460 ° F) do bodu tání (1 541 ° C nebo 2 806 ° F). Při tlacích přesahujících 186 kilobarů se stává supravodivý při -273,1 ° C (-459,6 ° F).
Poté, co ruský chemik Dmitrij Ivanovič Mendelejev v roce 1871 předpověděl existenci tohoto prvku, pokusně jej nazval ekaboron, švédský chemik Lars Fredrik Nilson v roce 1879 objevil jeho oxid, skandii, v minerálech vzácných zemin gadolinit a euxenit a švédský chemik Per Teodor Cleve později v roce 1879 identifikoval skandium jako hypotetický ekaboron. Skandium se vyskytuje v malých poměrech, obvykle méně než 0,2 procenta, v mnoha těžkých lanthanidových rudách a v mnoha cínových, uranových a wolframových rudách. Thortveitit (skandium silikát) je jediný minerál obsahující velké množství skandia, asi 34 procent, ale bohužel je tento minerál poměrně vzácný a není důležitým zdrojem skandia. Kosmická hojnost skandia je relativně vysoká. Přestože se jedná pouze o 50. nejhojnější prvek na Zemi (jeho hojnost je podobná jako u berylia), jedná se o 23. nejhojnější prvek na slunci.
Skandium v přírodě existuje ve formě jednoho stabilního izotopu, skandia-45. Z 25 radioaktivních izotopů (s výjimkou jaderných izomerů) s hmotností v rozmezí 36 až 61 je nejstabilnější skandium-46 (poločas 83,79 dní) a nejméně stabilní je skandium-39 (poločas méně než 300 nanosekund)).
Skandium se oddělí od ostatních vzácných zemin srážením nerozpustného síranu skandia draselného nebo extrakcí thiokyanátu skandia diethyletherem. Samotný kov byl poprvé připraven v roce 1938 elektrolýzou chloridů draslíku, lithia a skandia v eutektické směsi (tj. Směs s nejnižšími možnými teplotami tání s těmito složkami). Skandium se nyní vyrábí převážně jako vedlejší produkt extrakce uranu z minerálního daviditu, který obsahuje asi 0,02% oxidu skandia. Skandium existuje ve dvou allotropických (strukturálních) formách. A-fáze je těsně uzavřena hexagonální s a = 3,3088 Á a c = 5,2680 Á při pokojové teplotě. P-fáze je kubická soustava zaměřená na tělo s odhadem a = 3,73 Á při 1 337 ° C (2 439 ° F).
Bylo vyvinuto pouze několik použití tohoto neobvyklého přechodného kovu, většinou kvůli omezené dostupnosti a vysokým nákladům skandia. Její nízká hustota a vysoká teplota tání naznačují aplikace jako legovací činidlo pro lehké kovy pro vojenské a vysoce výkonné aplikace. Hlavní použití skandia je jako přísada do slitin na slitinách na bázi hliníku pro sportovní potřeby a halogenidové výbojky s vysokou intenzitou. Když je skandium legováno hliníkem a slitinami na bázi hliníku, omezuje růst zrna při vysoké teplotě.
Chemie skandia nese bližší podobnost s chemií ostatních prvků vzácných zemin oxidačního stavu +3 než chemie hliníku nebo titanu. Část jeho chování je však pro vzácné zeminy atypická, protože má výrazně menší iontový poloměr (1,66 Á pro koordinační číslo 12) ve srovnání s průměrem vzácných zemin (1,82 Á pro koordinační číslo 12). Z tohoto důvodu je iont Sc 3+ relativně silná kyselina a má mnohem větší tendenci tvořit komplexní ionty.
Vlastnosti prvku
| protonové číslo | 21 |
|---|---|
| atomová hmotnost | 44,95591 |
| bod tání | 1 541 ° C (2 806 ° F) |
| bod varu | 2 836 ° C (5 137 ° F) |
| specifická gravitace | 2,989 (24 ° C nebo 75 ° F) |
| oxidační stav | +3 |
| elektronová konfigurace | [Ar] 3d 1 4s 2 |




![Velký iluzní film od Renoira [1937] Velký iluzní film od Renoira [1937]](https://images.thetopknowledge.com/img/entertainment-pop-culture/9/grand-illusion-film-renoir-1937.jpg)